
Содержание
Атомный номер соответствует количеству протонов в ядре отдельного атома элемента. Это значение не меняется; следовательно, вы можете использовать его для определения других характеристик изотопа, таких как количество нейтронов.
Шаги
Часть 1 из 2: Определение атомного номера
Найдите копию таблицы Менделеева. Щелкните здесь, если у вас его нет. У каждого элемента есть свой атомный номер; таким образом, нет никаких сокращений для изучения содержания. Воспользуйтесь копией таблицы или попробуйте ее запомнить.
- У большинства книг по химии таблица напечатана на задней обложке.

Найдите в таблице изучаемый элемент. Большинство таблиц включают полное название элементов, а также их символы (например, Hg для ртути). Если вы не можете найти то, что ищете, зайдите в Интернет и выполните поиск по термину «химический символ» и имени элемента.
Найдите атомный номер элемента. Обычно он находится в верхнем левом или правом углу дома элемента, но может быть и в других местах. Кроме того, это всегда целое число.- Если число включает десятичную точку, это, вероятно, указывает на атомную массу.
Подтвердите информацию по элементам рядом. Таблица Менделеева организована согласно порядку атомных номеров. Например, если ваш изотопный номер «33», элемент слева будет «32», а элемент справа - «34». В этом случае это потому, что вы смотрите на атомный номер.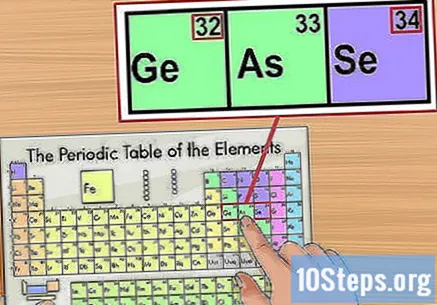
- Есть скачок между элементами «56» (барий) и «88» (радио). Изотопы, соответствующие этому диапазону, находятся в двух строках под таблицей. Они только так разделяются, чтобы таблица не была слишком большой.
Понять, что означает атомный номер. Атомный номер имеет простое определение: количество протонов в атоме элемента. Это количество протонов, в свою очередь, определяет общий электрический заряд ядра, который, следовательно, определяет, сколько электронов может зарядить атом. Поскольку электроны ответственны почти за все химические взаимодействия, атомный номер косвенно влияет на физические и химические свойства элемента.- Другими словами, каждый атом с восемью протонами соответствует атому кислорода. Два атома кислорода могут иметь разное количество нейтронов или (если один ион) или электронов, но у каждого из них всегда будет по восемь протонов.
Часть 2 из 2: поиск более важной информации
Определите атомный вес. Обычно он идет под названием элемента в периодической таблице и имеет два или три десятичных знака. Атомный вес соответствует средней массе атомов элемента, представляя, как он встречается в природе. Он измеряется в «атомных единицах массы» («u» или «u.m.a»).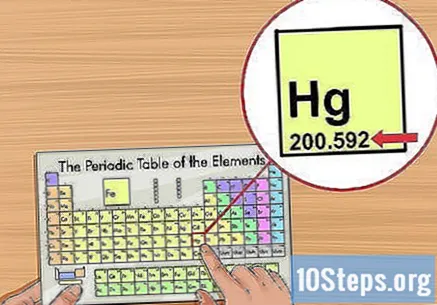
- Многие ученые предпочитают использовать термин «атомная масса» вместо веса.
Понять атомную массу. Понятие атомной массы очень похоже на понятие веса. Разница в том, что вес указывает на среднюю массу любого атома в элементе, а не конкретного атома. Например: грамм железа содержит несколько атомов с разной массой; вес указывает их «относительную массу». Если вы изучаете отдельный атом элемента, вам просто нужно знать его удельную массу.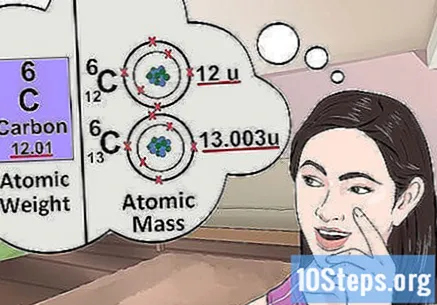
- Как правило, химические задачи, связанные только с атомами, уже определяют массовое атомное число. Вам просто нужно понять концепцию, чтобы не быть застигнутым врасплох, когда вы увидите другую ценность.
Округлить массовое число. Массовое число соответствует общему количеству протонов и нейтронов в атоме элемента. Подсчитать это несложно: достаточно взять атомную массу, указанную в периодической таблице, и округлить ее до ближайшего целого значения.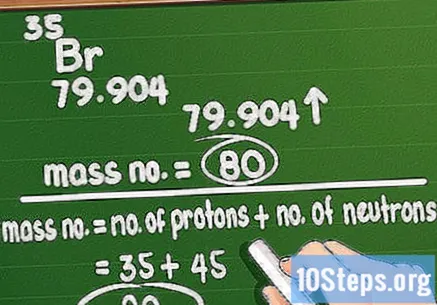
- Это работает, потому что количество нейтронов и протонов очень близко к 1 мкм, а количество электронов очень близко к нулю. Атомная масса включает точные вычисления для определения десятичного значения, но единственные данные, которые имеют значение, - это целые числа, которые говорят вам, сколько существует протонов и нейтронов.
- Помните, что если вы используете атомную массу, вы не сможете повлиять на вес конкретного атома в элементе. Например, образец брома имеет атомную массу 79 или 81.
Подсчитайте количество нейтронов. Вы уже знаете, что атомный номер равен количеству протонов, а массовое число равно сумме количества протонов и нейтронов. Чтобы определить количество нейтронов в элементе, просто вычтите атомный номер из общей массы. Некоторые примеры:
- Атом гелия (He) имеет массовое число 4 и атомный номер 2. Следовательно, 4 - 2 = 2 нейтрона.
- Образец серебра (Ag) имеет среднее массовое число 108 (согласно периодической таблице) и атомный номер 47. В среднем каждый атом в образце имеет 108 - 47 = 61 нейтрон.
Понять изотопы. Изотоп - это особая форма элемента, который содержит несколько нейтронов. Если проблема, которую вы хотите решить, вызывает что-то вроде «бор-10» или «B», это потому, что вы говорите об элементах бора с массовым числом 10. Используйте это значение, а не «нормальные» значения. бора.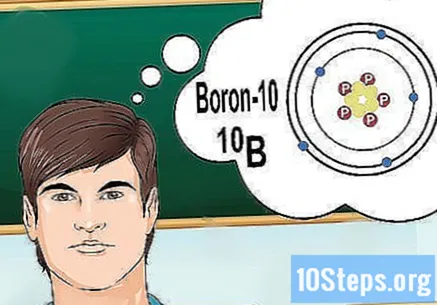
- Атомный номер изотопов никогда не меняется. Каждый изотоп элемента имеет одинаковое количество протонов.
подсказки
- Атомный вес некоторых более тяжелых элементов указан в круглых или квадратных скобках. Это означает, что этот вес является точной массой наиболее стабильного изотопа, а не средней массой нескольких изотопов. Наконец, это не влияет на атомный номер элемента.


