Содержание
В химии «парциальное давление» относится к давлению, которое каждый газ в газовой смеси оказывает на окружающую среду, такую как баллон с пробой, баллон с воздухом для дайвинга или пределы атмосферы. Вы можете рассчитать давление каждого газа в смеси, если знаете, сколько его имеется, какой объем он занимает и его температуру. Затем вы можете сложить эти парциальные давления, чтобы найти полное давление газовой смеси, или вы можете сначала найти общее давление, а затем найти парциальные давления.
Шаги
Часть 1 из 3: Понимание свойств газов
Рассматривайте каждый газ как «идеальный» газ. В химии идеальный газ - это газ, который взаимодействует с другими газами, не притягиваясь к своим молекулам. Отдельные молекулы могут сталкиваться друг с другом и отскакивать, как бильярдные шары, без какой-либо деформации.
- Идеальные давления газа увеличиваются, когда они сжимаются в меньшие пространства, и уменьшаются, когда они расширяются на большие площади. Эти отношения называются законом Бойля в честь Роберта Бойля. Математически это описывается как k = P x V или, проще говоря, k = PV, где k представляет постоянное соотношение, P представляет давление, а V представляет объем.
- Давление можно определить с помощью одной из нескольких возможных единиц. Один из них - Паскаль (Па), определяемый как сила Ньютона, приложенная к квадратному метру. Другой - атмосфера (атм), определяемая как давление атмосферы Земли на уровне моря. Давление 1 атм равно 101,325 Па.
- Идеальные температуры газа увеличиваются по мере увеличения и уменьшения объемов. Это соотношение называется законом Чарльза в честь Жака Шарля и математически описывается как k = V / t, где k представляет собой отношение между постоянным объемом и температурой, V снова представляет объем, а T представляет температуру.
- Температуры газа в этом уравнении даны в градусах Кельвина, которые находятся путем прибавления 273 к числу градусов Цельсия температуры газа.
- Эти два отношения можно объединить в одно уравнение: k = PV / T, которое также можно записать как PV = kT.

Определите, в каких количествах измеряются газы. У газов есть масса и объем. Объем обычно измеряется в литрах (л), но есть два типа массы.- Обычная масса измеряется в граммах или, если масса достаточно большая, в килограммах.
- Из-за легкости газов они также измеряются в другой форме массы, называемой молекулярной массой или молярной массой. Молярная масса определяется как сумма атомных весов каждого атома соединения, из которого состоит газ, по сравнению со значением 12 для углерода.
- Поскольку атомы и молекулы слишком малы для работы, количество газов определяется в молях. Количество молей, присутствующих в данном газе, можно определить путем деления массы на молярную массу и может быть представлено буквой n.
- Мы можем заменить произвольную константу k в уравнении газа произведением n, числа молей (моль) и новой константы R. Теперь уравнение можно записать nR = PV / T или PV = nRT.
- Значение R зависит от единиц измерения давления, объема и температуры газов. Для определения объема в литрах, температуры в Кельвинах и давления в атмосферах его значение составляет 0,0821 л атм / кмоль. Это также может быть записано L 0,0821 атм K моль, чтобы избежать разделительной полосы в единицах измерения.

Понять закон парциальных давлений Дальтона. Закон Дальтона, разработанный химиком и физиком Джоном Дальтоном, который первым выдвинул идею о том, что химические элементы состоят из атомов, гласит, что полное давление газовой смеси является суммой давлений каждого из газов в смеси.- Закон Дальтона можно записать в виде уравнения P общий = P1 + P2 + P3... с таким количеством добавлений после знака равенства, сколько газов в смеси.
- Уравнение закона Дальтона может быть расширено при работе с газами, индивидуальные парциальные давления которых неизвестны, но нам известны их объем и температура. Парциальное давление газа - это то же самое давление, если бы такое же количество газа было единственным газом в контейнере.
- Для каждого из парциальных давлений мы можем переписать уравнение идеального газа так, чтобы вместо формулы PV = nRT мы могли иметь только P слева от знака равенства. Для этого мы делим обе стороны на V: PV / V = nRT / V. Две V на левой стороне компенсируют друг друга, оставляя P = nRT / V.
- Затем мы можем заменить каждый P, указанный в правой части уравнения парциального давления: Pобщий = (nRT / V) 1 + (nRT / V) 2 + (nRT / V) 3…
Часть 2 из 3: Расчет парциальных давлений, а затем общего давления

Определите уравнение парциального давления для газов, с которыми вы работаете. Для целей этого расчета мы предположим, что баллон объемом 2 литра содержит три газа: азот (N2), кислород (O2) и диоксид углерода (CO2). Каждого из газов по 10 г, и температура каждого из них в колбе 37º по Цельсию. Нам нужно найти парциальное давление каждого газа и полное давление, которое смесь оказывает на контейнер.- Наше уравнение парциального давления становится P общий = P азот + P кислород + P углекислый газ .
- Поскольку мы пытаемся найти давление, которое оказывает каждый газ, мы знаем объем и температуру, и мы можем определить, сколько молей каждого газа присутствует в зависимости от массы, мы можем переписать это уравнение как: Pобщий = (nRT / V) азот + (nRT / V) кислород + (nRT / V) углекислый газ

Переведите температуру в Кельвин. Температура составляет 37º по Цельсию, поэтому прибавьте 273 к 37, чтобы получить 310 К.
Найдите количество молей для каждого газа в образце. Число молей газа - это масса газа, деленная на его молярную массу, которая, как мы сказали, является суммой атомных масс каждого атома в соединении.
- Для первого газа азот (N2), каждый атом имеет атомный вес 14. Поскольку азот двухатомный (молекулярная форма двух атомов), мы должны умножить 14 на 2, чтобы найти, что азот в нашем образце имеет молярную массу 28. Затем разделите массу в граммах, 10 г, на 28, чтобы получить количество молей, которое мы приблизим к 0,4 моль азота.
- Для второго газа кислород (O2), каждый атом имеет атомный вес 16. Кислород также двухатомный, поэтому умножьте 16 на 2, чтобы найти, что кислород в нашем образце имеет молярную массу 32. Деление 10 г на 32 дает нам примерно 0,3 моль кислорода в нашем образце. образец.
- Третий газ - углекислый газ (CO2), имеет 3 атома: один углерод с атомной массой 12; и два кислорода, каждый с атомным весом 16. Мы складываем три веса: 12 + 16 + 16 = 44 для молярной массы. Разделив 10 г на 44, мы получим примерно 0,2 моль диоксида углерода.

Замените значения молями, объемом и температурой. Наше уравнение теперь выглядит так: Pобщий = (0,4 * R * 310/2) азот + (0,3 * R * 310/2) кислород + (0,2 * R * 310/2) углекислый газ.- Для простоты мы исключили единицы измерения, сопровождающие значения. Эти единицы будут отменены после того, как мы выполним математические вычисления, и останется только единица измерения, которую мы используем для отчета о давлении.
Подставьте значение константы R. Мы найдем парциальное и полное давление в атмосферах, поэтому будем использовать значение R 0,0821 атм л / кмоль. Подстановка значения в уравнение теперь дает нам Pобщий =(0,4 * 0,0821 * 310/2) азот + (0,3 *0,0821 * 310/2) кислород + (0,2 * 0,0821 * 310/2) углекислый газ .
Рассчитайте парциальные давления для каждого газа. Теперь, когда у нас есть значения, пора заняться математикой.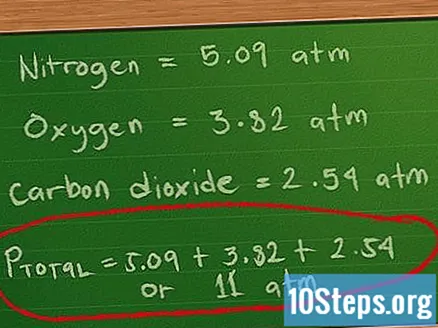
- Для парциального давления азота мы умножаем 0,4 моль на нашу константу 0,0821 и нашу температуру 310 K, а затем делим на 2 литра: примерно 0,4 * 0,0821 * 310/2 = 5,09 атм.
- Для парциального давления кислорода мы умножаем 0,3 моль на нашу константу 0,0821 и нашу температуру 310 K, а затем делим на 2 литра: 0,3 * 0,0821 * 310/2 = 3,82 атм, приблизительно.
- Для парциального давления углекислого газа мы умножаем 0,2 моль на нашу константу 0,0821 и нашу температуру 310 K, а затем делим на 2 литра: 0,2 * 0,0821 * 310/2 = 2,54 атм, приблизительно.
- Теперь сложим эти давления, чтобы найти полное давление: Pобщий = 5,09 + 3,82 + 2,54, или примерно 11,45 атм.
Часть 3 из 3: Расчет общего давления, а затем парциальных давлений
Задайте уравнение парциального давления, как и раньше. Опять же, мы предполагаем, что колба на 2 литра содержит 3 газа: азот (N2), кислород (O2) и диоксид углерода (CO2). По 10 г каждого из газов, температура каждого из газов в колбе составляет 37 градусов Цельсия.
- Температура в Кельвине по-прежнему будет 310, и, как и прежде, у нас будет около 0,4 моль азота, 0,3 моль кислорода и 0,2 моль диоксида углерода.
- Точно так же мы все еще найдем давление в атмосферах, поэтому мы будем использовать значение 0,0821 атм л / кмоль для постоянной R.
- Итак, наше уравнение парциального давления на этом этапе все еще выглядит так же: Pобщий =(0,4 * 0,0821 * 310/2) азот + (0,3 *0,0821 * 310/2) кислород + (0,2 * 0,0821 * 310/2) углекислый газ.
Сложите количество молей каждого из газов в образце, чтобы найти общее количество молей газовой смеси. Поскольку объем и температура одинаковы для каждой пробы в газе, не говоря уже о том, что каждое молярное значение умножается на одну и ту же константу, мы можем использовать распределительное свойство математики, чтобы переписать уравнение как Pобщий = (0,4 + 0,3 + 0,2) * 0,0821 * 310/2.
- Добавление 0,4 + 0,3 + 0,2 = 0,9 моль газовой смеси. Это еще больше упрощает уравнение для P общий = 0,9 * 0,0821 * 310/2.
Рассчитайте полное давление газовой смеси. Умножая 0,9 * 0,0821 * 310/2 = 11,45 моль, приблизительно.
Найдите долю каждого газа в общей смеси. Для этого разделите количество молей каждого из газов на общее количество молей.
- Здесь 0,4 моль азота, поэтому 0,4 / 0,9 = 0,44 (44%) образца, приблизительно.
- Азот составляет 0,3 моль, поэтому примерно 0,3 / 0,9 = 0,33 (33%) образца.
- Имеется 0,2 моль диоксида углерода, так что 0,2 / 0,9 = 0,22 (22%) образца приблизительно.
- Хотя приблизительные проценты выше в сумме составляют всего 0,99, фактические десятичные дроби повторяются, поэтому фактическая сумма представляет собой серию повторений девяток после десятичной дроби. По определению это то же самое, что 1 или 100%.
Умножьте пропорциональное значение каждого газа на общее давление, чтобы найти парциальное давление.
- Умножая 0,44 * 11,45 = 5,04 атм, приблизительно.
- Умножая 0,33 * 11,45 = 3,78 атм, приблизительно.
- Умножая 0,22 * 11,45 = 2,52 атм, приблизительно.
подсказки
- Вы заметите небольшую разницу в значениях, если сначала определите парциальные давления, затем общее давление и сначала определите полное давление, а затем парциальные давления. Помните, что данные значения были представлены как приблизительные значения из-за округления до одного или двух десятичных знаков, чтобы значения было легче понять. Если вы будете производить расчеты с помощью калькулятора без округления, вы заметите небольшое расхождение между двумя методами, если оно вообще есть.
Предупреждения
- Знание парциального давления газа может стать вопросом жизни и смерти для дайверов. Слишком низкое парциальное давление кислорода может привести к потере сознания и смерти, в то время как очень высокое парциальное давление водорода или кислорода также может быть токсичным.
Необходимые материалы
- Калькулятор;
- Справочник атомных масс / молярных масс.